К получению раствора с ![]() может привести растворение в воде вещества, формула которого:
может привести растворение в воде вещества, формула которого:
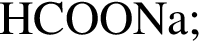

Решение. Рассмотрим предложенные взаимодействия:
1. Хлорид натрия является солью сильного основания и сильной кислоты, поэтому в растворе гидролизу не подвергается, реакция среды — нейтральная, 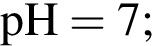
2. Натрий при растворении в воде образует щелочь, среда щелочная, поэтому 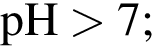
3. При растворении ![]() в воде образуется фосфорная кислота,
в воде образуется фосфорная кислота, 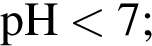
4. Формиат натрия является солью сильного основания и слабой кислоты, в растворе подвергается гидролизу по аниону, поэтому среда слабощелочная, 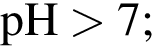
5. Нитрат калия является солью сильного основания и сильной кислоты, поэтому в растворе гидролизу не подвергается, реакция среды — нейтральная, 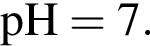
Правильный ответ указан под номером 3.

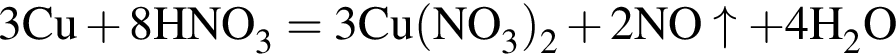
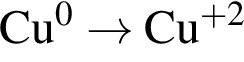 ).
).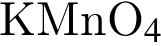 НЕ обесцвечивает вещество:
НЕ обесцвечивает вещество: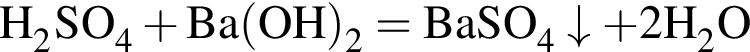 — выпадает белый плотный осадок сульфата бария;
— выпадает белый плотный осадок сульфата бария;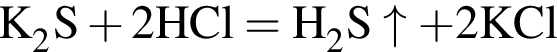 — выделяется сероводород (бесцветный газ с характерным резким запахом);
— выделяется сероводород (бесцветный газ с характерным резким запахом);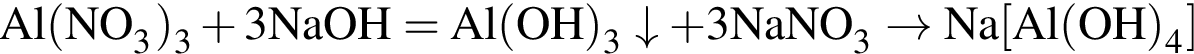 — выпадает белый осадок гидроксида алюминия, растворяющийся в избытке щёлочи;
— выпадает белый осадок гидроксида алюминия, растворяющийся в избытке щёлочи;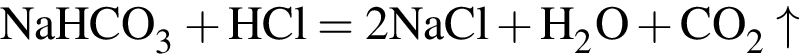 — выделяется углекислый газ (без запаха и цвета, не поддерживающий горение).
— выделяется углекислый газ (без запаха и цвета, не поддерживающий горение).
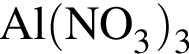 . Его молярная масса: M = 27 + 14·3 + 16·9 = 213, поэтому
. Его молярная масса: M = 27 + 14·3 + 16·9 = 213, поэтому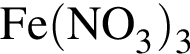 . Его молярная масса: M = 56 + 14·3 + 16·9 = 242, поэтому
. Его молярная масса: M = 56 + 14·3 + 16·9 = 242, поэтому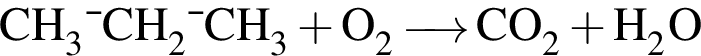
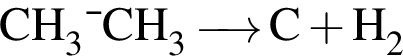
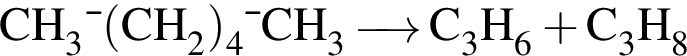
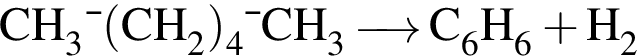



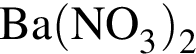
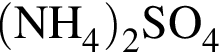 →
→ 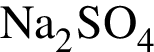
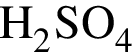
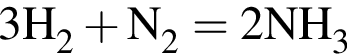
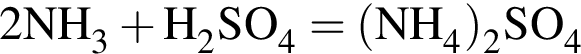
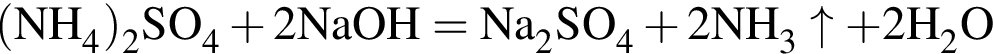
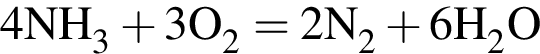
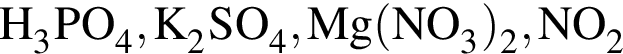 , с которыми реагирует разбавленный водный раствор
, с которыми реагирует разбавленный водный раствор 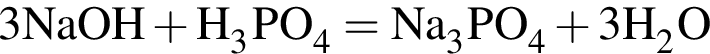
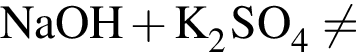
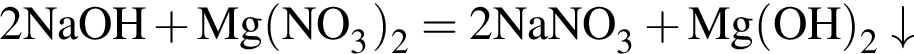
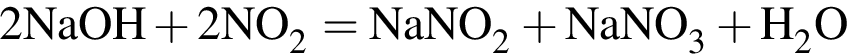
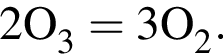
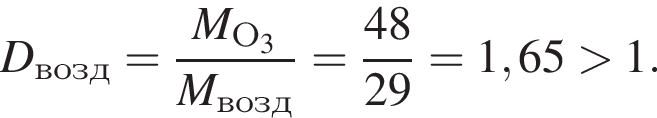
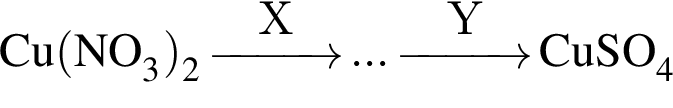
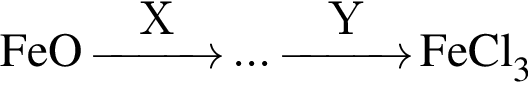
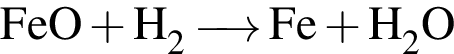
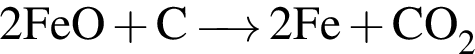
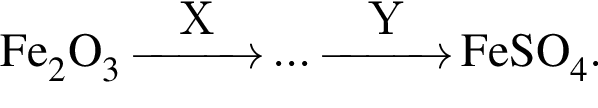 Обе реакции являются окислительно восстановительными. Реагентами X и У могут быть:
Обе реакции являются окислительно восстановительными. Реагентами X и У могут быть: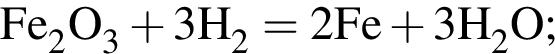
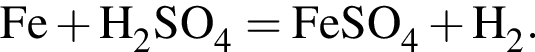
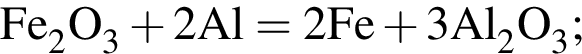
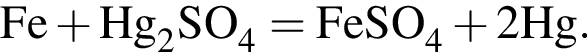
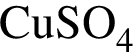 6% добавили медный купорос массой 75 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю(%) соли в полученном растворе.
6% добавили медный купорос массой 75 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю(%) соли в полученном растворе.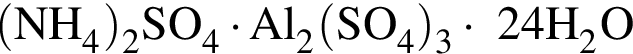 равно:
равно: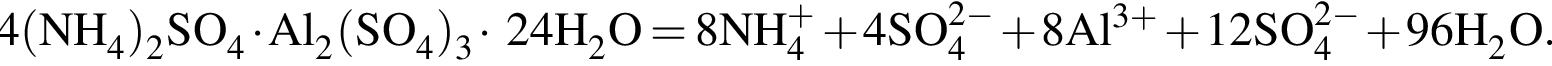

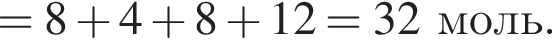

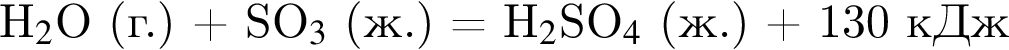
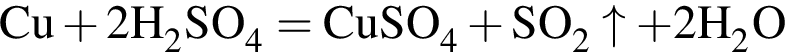 — кислотный оксид серы (IV);
— кислотный оксид серы (IV);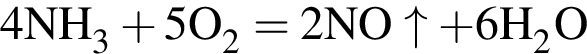 — несолеобразующий оксид азота (II);
— несолеобразующий оксид азота (II);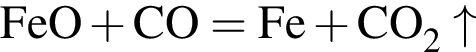 — кислотный оксид углерода (IV);
— кислотный оксид углерода (IV);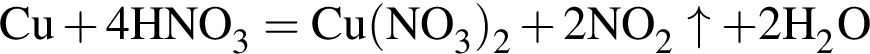 — кислотный оксид азота (IV).
— кислотный оксид азота (IV).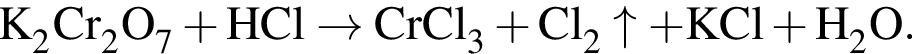
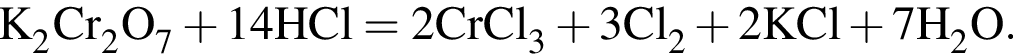
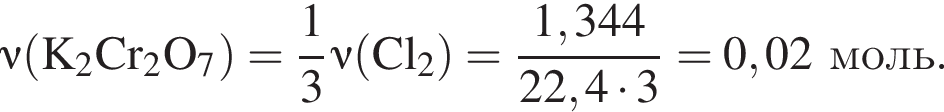
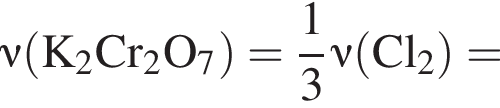
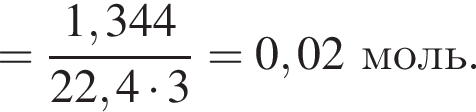
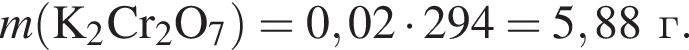
 с выделением газа.
с выделением газа. 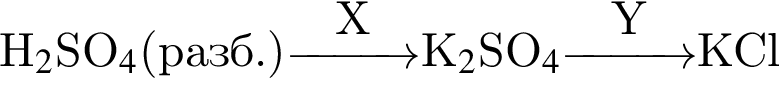
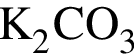 и
и 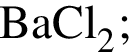
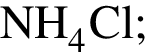
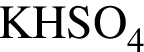 и
и 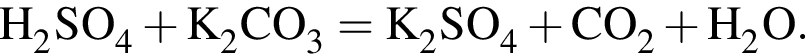
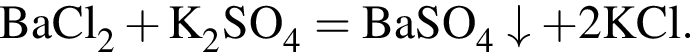
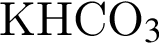 с выделением газа;
с выделением газа; ↑,
↑, ↑.
↑.
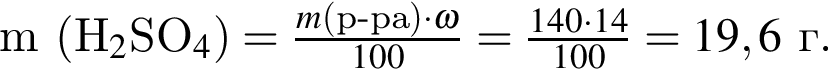
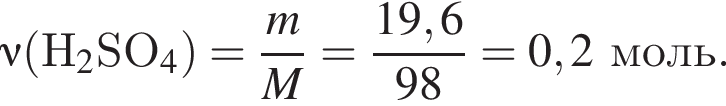
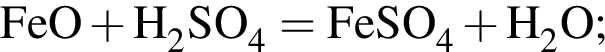
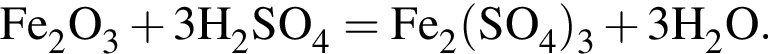
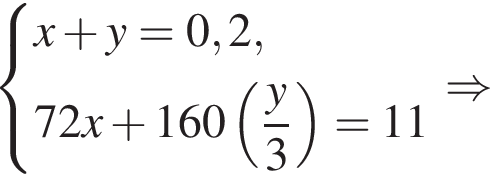
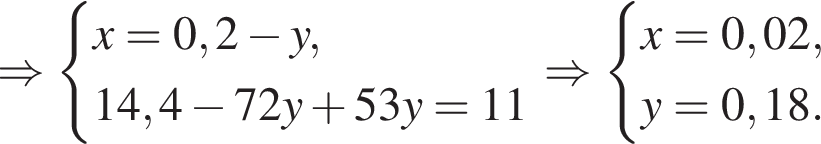
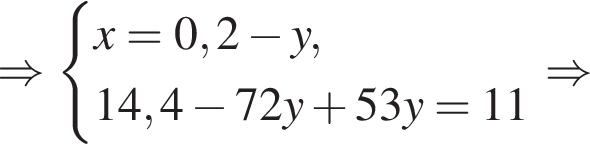
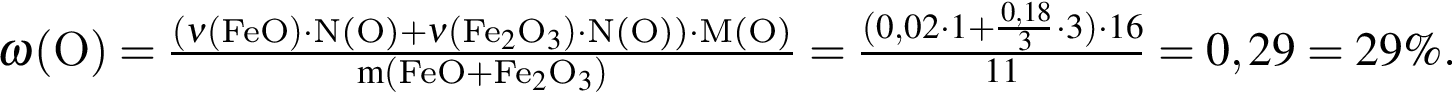
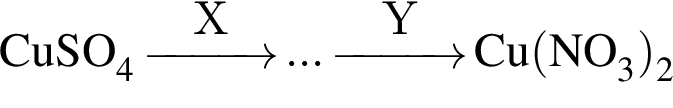
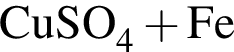 →
→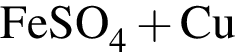
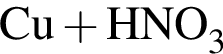 →
→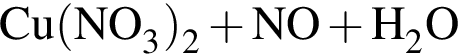
 .
.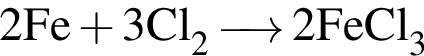 .
. .
.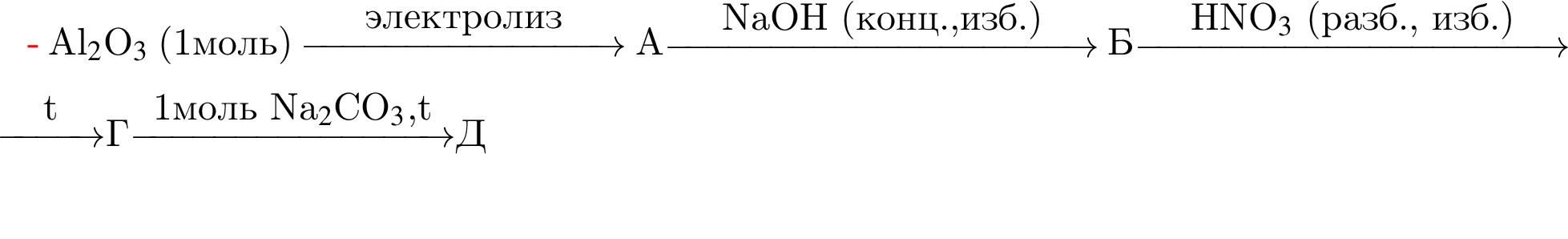
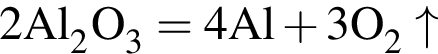
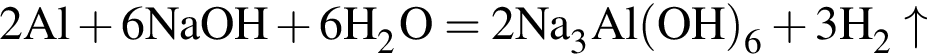
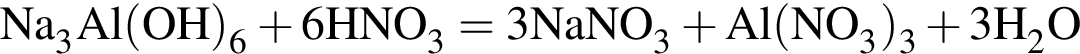
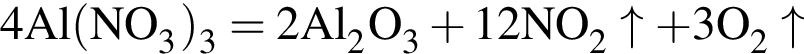
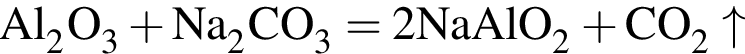



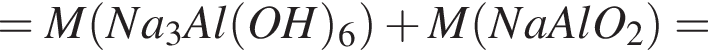
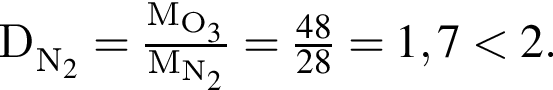
 массовая доля кислорода составляет:
массовая доля кислорода составляет:  Массовая доля цинка больше массовой доли кислорода в
Массовая доля цинка больше массовой доли кислорода в 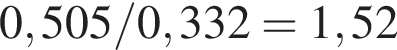 раз.
раз.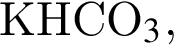 верно:
верно: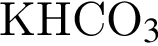 не взаимодействует с углекислым газом, являясь кислой солью.
не взаимодействует с углекислым газом, являясь кислой солью.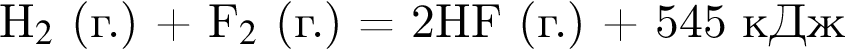


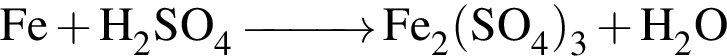
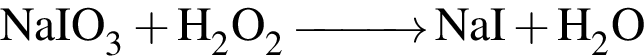

 ↑
↑ ↑
↑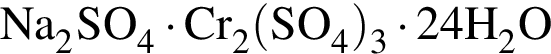 равно:
равно: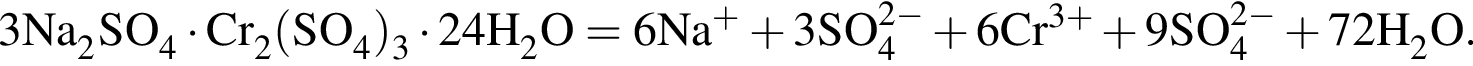
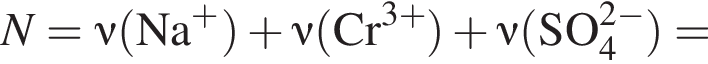
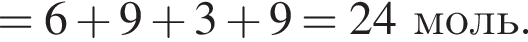
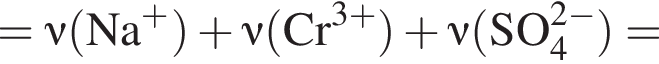
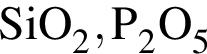 ;
;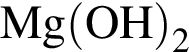 ;
;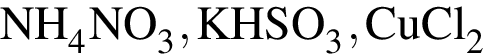 ;
;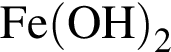 ;
;
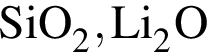 ;
;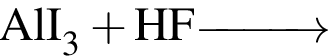
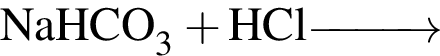
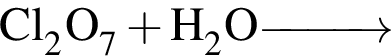
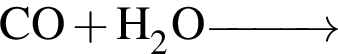
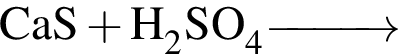
 — образуется одноосновная бескислородная кислота;
— образуется одноосновная бескислородная кислота; — образуется двухосновная кислородсодержащая кислота;
— образуется двухосновная кислородсодержащая кислота;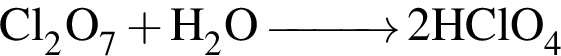 — образуется одноосновная кислородсодержащая кислота;
— образуется одноосновная кислородсодержащая кислота;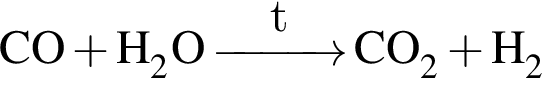 — кислота не образуется;
— кислота не образуется; — образуется бескислородная двухосновная кислота.
— образуется бескислородная двухосновная кислота.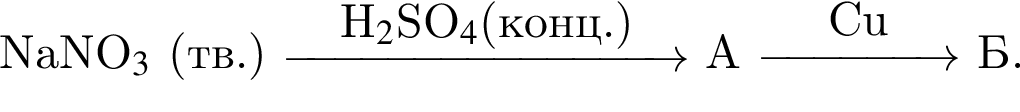
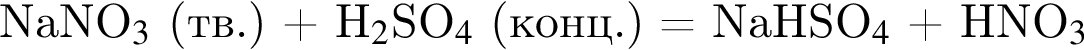
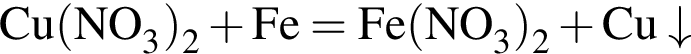


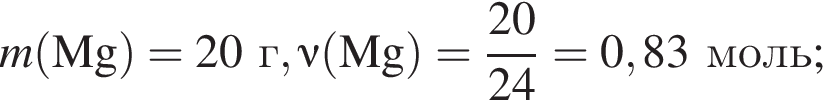
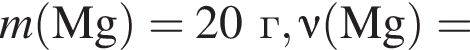
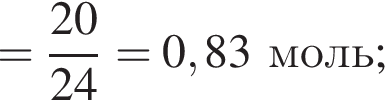
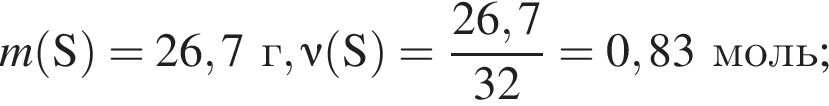
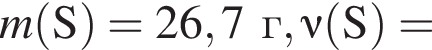
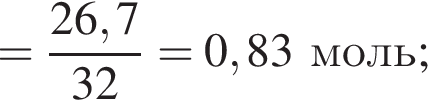
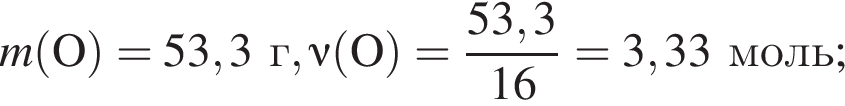
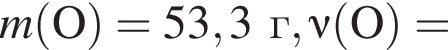
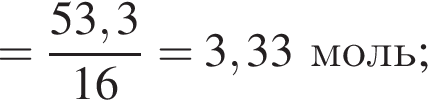
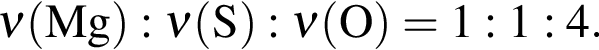
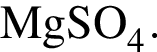
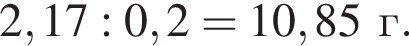 Тогда 10,85 г — это 34 % от того, что должен получать человек. Отсюда истинная масса сульфата магния на неделю составит
Тогда 10,85 г — это 34 % от того, что должен получать человек. Отсюда истинная масса сульфата магния на неделю составит 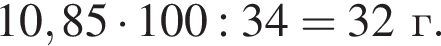
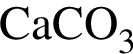
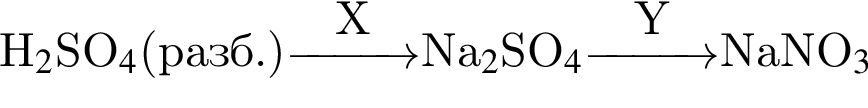
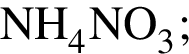

 и
и 
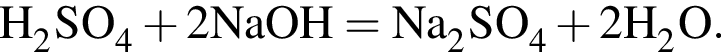
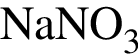 , нужен источник нитрат ионов. Обязательным условием реакции соли с солью является растворимость обеих солей, вступающих в реакцию, и выделение в ходе реакции осадка, газа или воды.
, нужен источник нитрат ионов. Обязательным условием реакции соли с солью является растворимость обеих солей, вступающих в реакцию, и выделение в ходе реакции осадка, газа или воды. 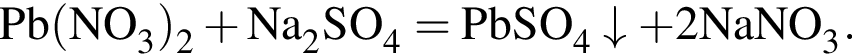
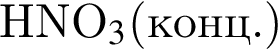
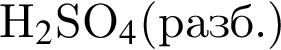
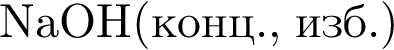
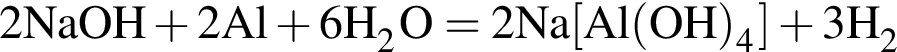
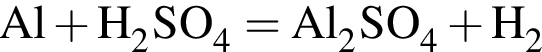
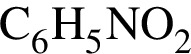 ;
;
 ). Далее из всех галогеноводородов нужно выбрать с наименьшей молярной массой, так как в таком случае количество вещества будет наибольшим. Самая маленькая молярная масса галогеноводородов из списка у соляной кислоты.
). Далее из всех галогеноводородов нужно выбрать с наименьшей молярной массой, так как в таком случае количество вещества будет наибольшим. Самая маленькая молярная масса галогеноводородов из списка у соляной кислоты.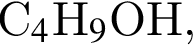 которые можно окислить до соответствующих альдегидов состава
которые можно окислить до соответствующих альдегидов состава 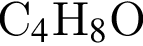 , равно:
, равно: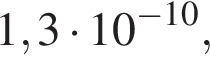 а уксусной
а уксусной 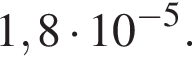
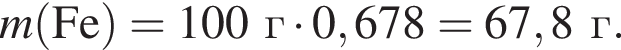
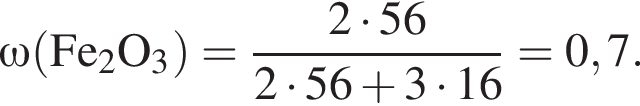


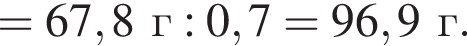
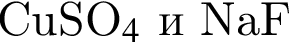
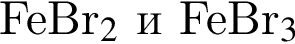
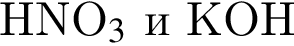
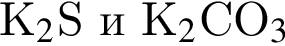
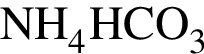
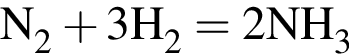 ;
; 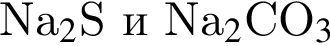
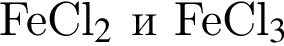
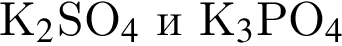
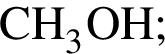
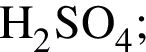
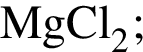
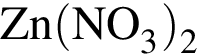 в растворе)=189x
в растворе)=189x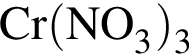
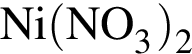
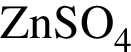
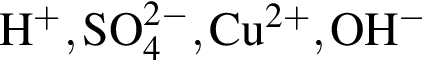 . В ходе опытов обнаружилось следующее:
. В ходе опытов обнаружилось следующее: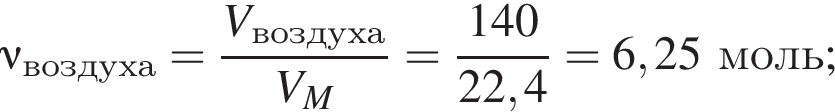
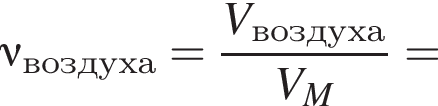
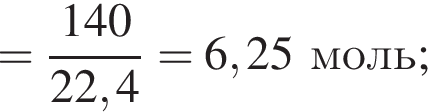




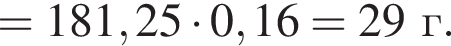

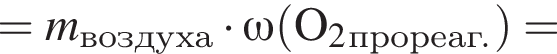
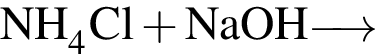
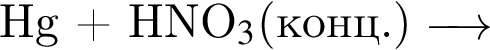
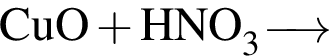
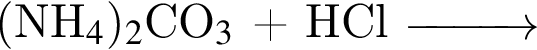
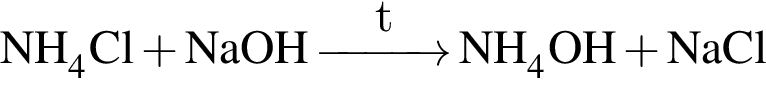
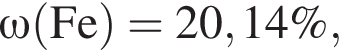
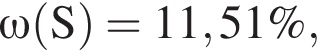
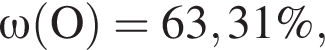
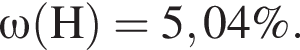 Вычислите массу (мг) кристаллогидрата в 300 г корма.
Вычислите массу (мг) кристаллогидрата в 300 г корма.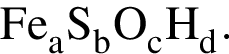 Найдем соотношение атомов железа, серы, кислорода и водорода в соединении:
Найдем соотношение атомов железа, серы, кислорода и водорода в соединении: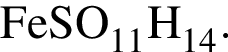 Это соответствует формуле гептагидрата сульфата железа(II) —
Это соответствует формуле гептагидрата сульфата железа(II) — 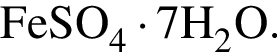
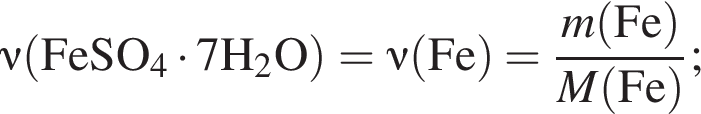
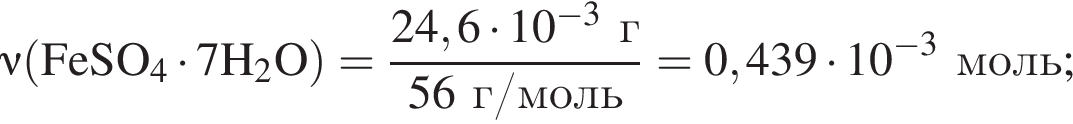
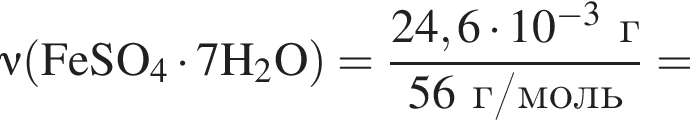
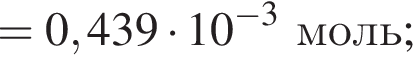
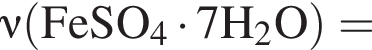
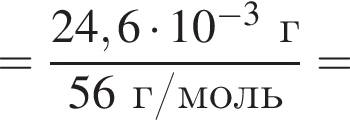
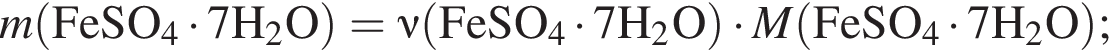
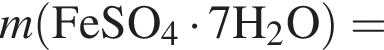
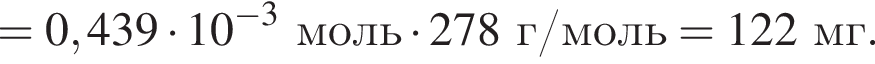

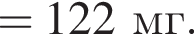
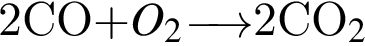 получается кислотный оксид.
получается кислотный оксид.
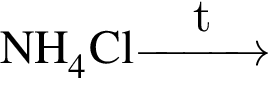
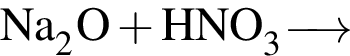
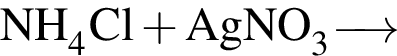
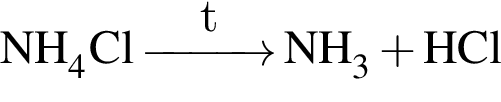
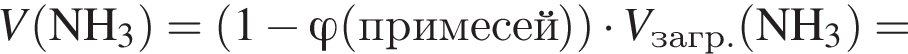
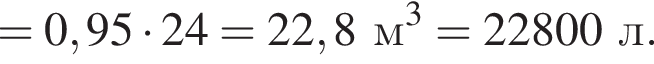


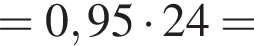
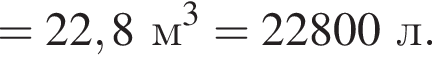
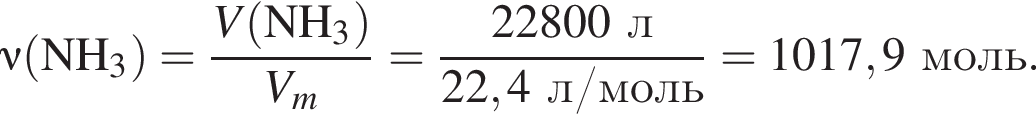
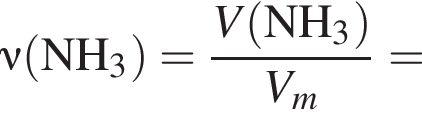
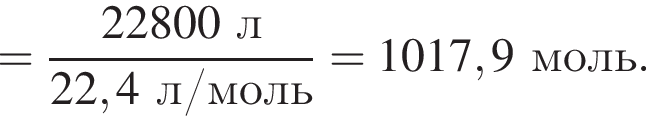
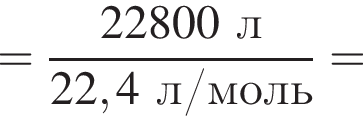
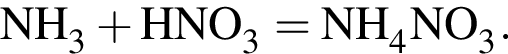

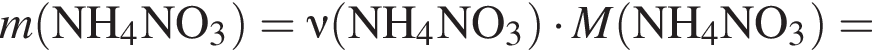

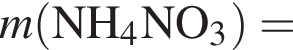
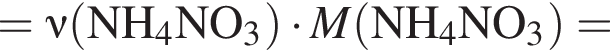
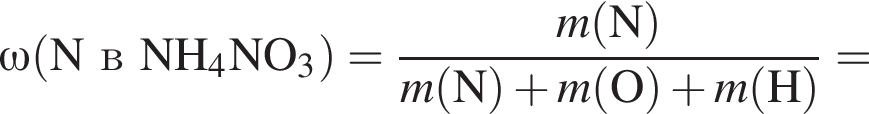
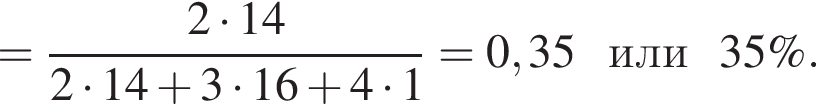

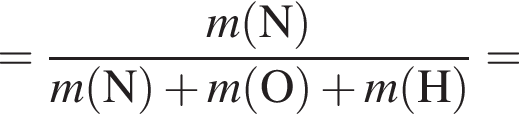


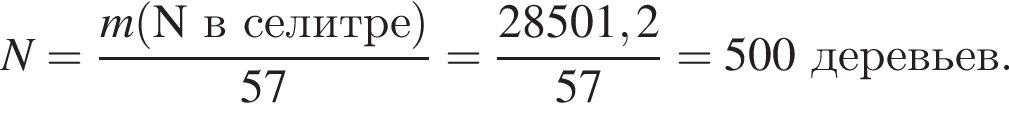

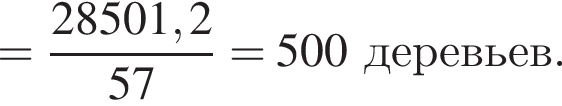
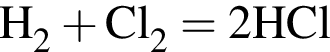 );
);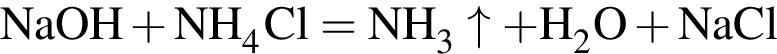 );
);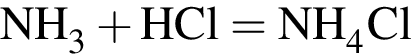 ).
).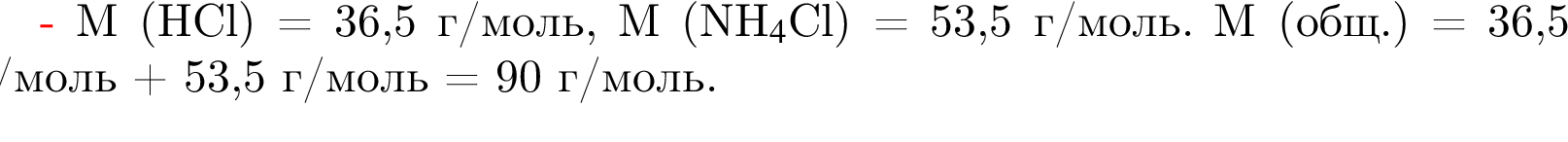
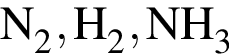 )=20,089−2n моль
)=20,089−2n моль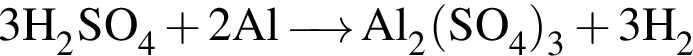
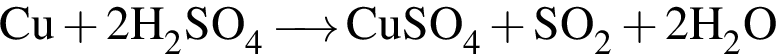
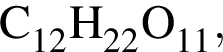 справедливо утверждение:
справедливо утверждение: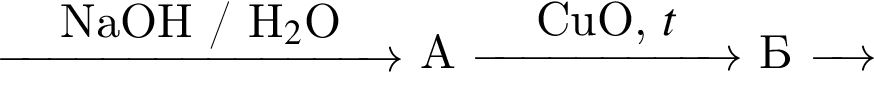
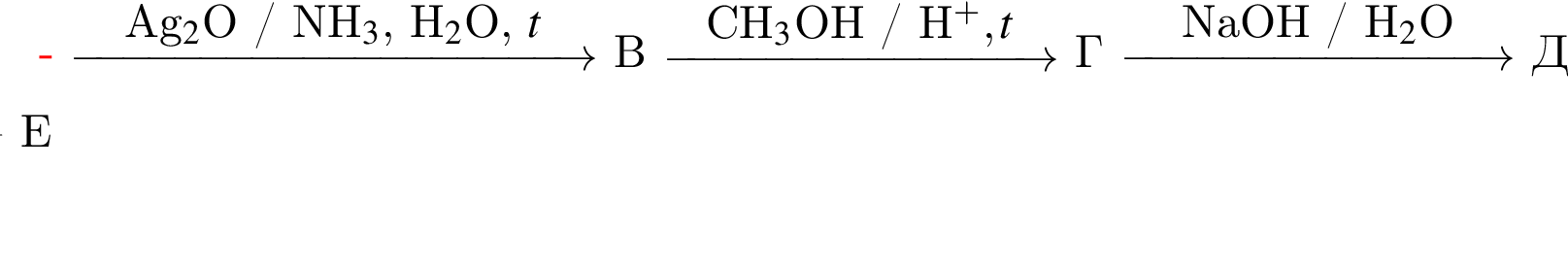
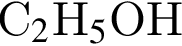 и ацетат натрия
и ацетат натрия 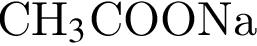
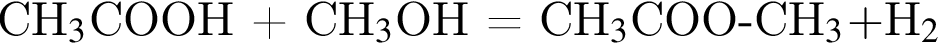
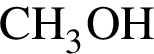 ( Молярная масса = 32 г/моль) и вещество «Е» - ацетат натрия
( Молярная масса = 32 г/моль) и вещество «Е» - ацетат натрия 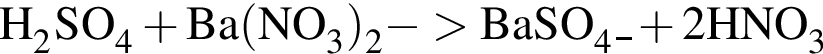
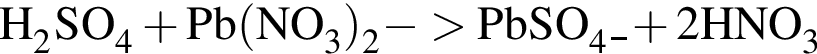
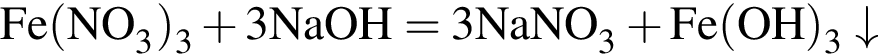 — выпадает бурый осадок гидроксида железа (III);
— выпадает бурый осадок гидроксида железа (III);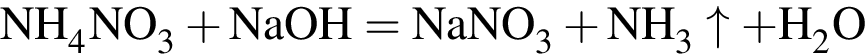 — выделяется аммиак (бесцветный газ с характерным резким запахом);
— выделяется аммиак (бесцветный газ с характерным резким запахом);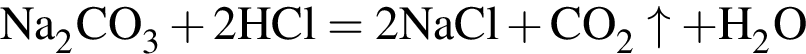 — выделяется углекислый газ (без запаха и цвета, не поддерживающий горение);
— выделяется углекислый газ (без запаха и цвета, не поддерживающий горение);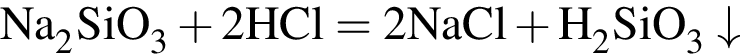 — выпадает кремниевая кислота (белый студенистый осадок).
— выпадает кремниевая кислота (белый студенистый осадок).